Processamento da amostra de sangue para hemograma: técnica
Diagnóstico das Doenças nas Aves – Exames Laboratoriais
O diagnóstico das doenças nas aves deve ser realizado considerando-se o histórico, exame clínico e os resultados dos exames laboratoriais. As amostras que podem ser obtidas das aves e utilizadas para exames laboratoriais são:
Fezes
Uratos
Sangue
Sêmen
Biópsias
Swabs
Aspirados
Penas
Raspados de pele
Cada amostra pode ser utilizada para vários exames. Nos últimos anos o conhecimento dos parâmetros normais em aves silvestres tem aumentado muito, principalmente nas aves de cativeiro, consequentemente, a interpretação dos resultados está mais fácil e confiável. Por exemplo, valores hematológicos e bioquímicos estão sendo estabelecidos para várias espécies. No Brasil, as publicações (artigos científicos, teses e dissertações) aumentaram nos últimos anos. O conhecimento dos valores normais é importante e há necessidade de ampliar os dados de valores normais para aves.
Regras gerais a serem aplicadas nas amostras para diagnóstico:
- regra geral: estar preparado para coletar sangue e outras amostras de cada ave; preparar os materiais como tubos, lâminas, frascos;
- utilizar materiais de boa qualidade: conferir o prazo de validade dos tubos com anticoagulantes; usar lâminas de vidro limpas;
- realizar as coletas das amostras com critério, eficiência e assegurar o bem-estar das aves; por exemplo, limitar o volume de sangue a ser coletado da ave, dependendo da condição do animal (ter certeza do volume de sangue que pode ser coletado da ave);
- identificar todos os tubos, frascos e lâminas com amostras e registrar os dados do animal;
- monitorar a ave após a coleta da amostra, observando sua recuperação. Ex.: tempo de sangramento prolongado após a coleta de sangue pode indicar intoxicação por dicumarol
AMOSTRA DE SANGUE
As amostras de sangue, soro e palsma são utilizadas em vários exames:
- Hematologia: sangue total para o hemograma, que é a avaliação quantitativa e qualitativa das células sanguíneas;
- Bioquímicos: soro e plasma, com análise e quantificação de várias substâncias, normais e anormais, como enzimas, metabólitos, proteínas, minerais;
- Parasitologia: detecção de protozoários parasitos ou outros parasitos, como microfilárias, na extensão sanguínea corada;
- Toxicologia: análise de toxinas;
- Microbiologia: detecção de bactérias e outros microrganismos no sangue; cultura;
- Reação em cadeia da polimerase: detecção do DNA de vários microrganismos;
- Hemogasometria: níveis de PO2 e PCO2
Antes da coleta de sangue, deve-se observar os cuidados necessários com a amostra, como uso ou não de anticoagulantes, e conservação.
Coleta de sangue de aves
O volume total de sangue de uma ave é aproximadamente 10% do seu peso corporal. Uma ave de 30 gramas tem aproximadamente 3,0 mL de sangue, e desse volume, considerando uma ave saudável, pode ser coletado com segurança até 10% (0,3 mL) de sangue. Esse volume deve ser reduzido na ave doente. O hemograma pode ser realizado com 0,3 mL de sangue.
Dessa forma, coletar o volume de sangue correspondente a 1% (ou menos), do peso corporal da ave saudável. Exemplos:
- Periquito de 80g – coletar até 0,8ml de sangue
- Pomba de 500 g: coletar até 5,0 ml
O sangue pode ser coletado de vários locais nas aves. A escolha do local depende da espécie da ave, local de preferência do veterinário, condição física do paciente e do volume de sangue necessário. O sangue venoso é a melhor amostra para exames hematológicos. O sangue coletado de capilares (ex.: do corte da unha), geralmente contém artefatos celulares como macrófagos e material não encontrado normalmente no sangue periférico e a distribuição das células não é normal.
O sangue coletado da ave para exame hematológico deve ser de origem venosa e na maioria das aves pode ser obtido da veia basílica (vena cutanea ulnaris superficialis), a veia da asa, que atravessa a superfície ventral da articulação umeral-rádio ulnar (cotovelo) imediatamente abaixo da pele. A veia jugular (vena jugularis dextra): geralmente a direita, que é maior que a esquerda ou a veia tibial caudal (vena metatarsalis plantaris superficialis): localizada no lado medial do tíbiotarso, acima da articulação tarsal
Na maioria das vezes, a contenção física é utilizada para a coleta de sangue, com a ave na posição dorsal. Nas espécies maiores (avestruz, por exemplo) pode-se utilizar um capuz.
Nesse tópico será abordada a Hematologia, disciplina que estuda as células sanguíneas e o tecido hematopoiético, que produz as células. A primeira descrição da citologia sanguínea de aves foi em 1961.
Há um aumento significativo no atendimento de aves silvestres e domésticas, e os exames laboratoriais estão sendo solicitados de maneira crescente. Os sinais clínicos em aves são inespecíficos e o exame físico fornece informações limitadas, assim, o hemograma é uma ferramenta utilizada como apoio no diagnóstico e nas pesquisas aplicadas à indústria de aves domésticas. Os valores hematológicos de referência têm sido estabelecidos para muitas espécies de aves, mas alguns valores podem variar com a idade, sexo, estação/ambiente e influência hormonal.
HEMATOLOGIA
Na Hematologia serão abordados os seguintes tópicos:
- Morfologia das células sanguíneas: descrição das células e as alterações. As fotos estão em “células sanguíneas”
- Processamento da amostra de sangue para hemograma: técnica
- Interpretação do hemograma: alterações das células sanguíneas na presença de anemia, inflamação, estresse
Amostras de Sangue
A amostra para o hemograma é o sangue total, que deve ser coletado com anticoagulante. Os anticoagulantes são substâncias utilizadas para evitar a coagulação sanguínea. O sangue total é estável por 24 horas em refrigeração, mas a extensão sanguínea deve ser feita imediatamente após a coleta do sangue, em lâmina limpa e seca. Se a amostra de sangue permanecer por muito tempo no anticoagulante e houver demora (mais de duas horas) para a confecção da extensão, ocorrem alterações na morfologia das células sanguíneas. As células sanguíneas (leucócitos) de aves podem romper com facilidade durante a confecção da extensão sanguínea, dificultando a identificação das células. Desta forma, a confecção da extensão sanguínea deve ser feita com cuidado, com volume adequado de sangue e sem apertar a lâmina extensora no sangue.
Após realizar a extensão, secar a lâmina ao ar e corar. Na extensão sanguínea corada é realizada a avaliação da morfologia dos eritrócitos, a contagem diferencial de leucócitos e a pesquisa de hemoparasitas.
Os anticoagulantes mais utilizados são o ácido diamino tetra acético (EDTA), a heparina e citrato de sódio. É importante ressaltar que o processamento da amostra de sangue para hemograma deve ser realizado em até 24 horas, porque após esse tempo, ocorrem alterações nos eritrócitos (hemólise) e nos leucócitos, inviabilizando a análise e interpretação dos resultados.
O sangue pode ser coletado em tubos com EDTA (1,5 mg/mL de sangue). Porém, em algumas espécies de aves (Corvidae, Gruidae, Struthionidae, Alcedinidae) o EDTA causa hemólise progressiva dos eritrócitos, sendo necessário utilizar a heparina lítica como anticoagulante.
As amostras de sangue de aves podem ser coletadas em seringas heparinizadas com heparina sódica (1000 UI) e depois a amostra é transferida para o tubo, com cuidado, para evitar hemólise.
O plasma é a parte líquida do sangue, com anticoagulante. O sangue deve ser coletado com anticoagulante e centrifugado. Após a centrifugação (por 10 minutos, 3000 rpm) retirar o sobrenadante (plasma). O plasma pode ser refrigerado ou congelado, e é utilizado para análises bioquímicas. Deve-se verificar a compatibilidade do anticoagulante com a prova bioquímica.
O soro é a parte líquida do sangue, e o sangue deve ser coletado sem anticoagulante. Após a coagulação, separar o soro. O soro pode ser refrigerado ou congelado, e é utilizado para análises bioquímicas.
Na coleta de sangue, cuidar no manuseio da amostra. Identificar os tubos, lâminas e frascos. Observar a quantidade de anticoagulante necessária para o volume de sangue a ser coletado. Após a coleta do sangue total, homogeneizar com cuidado o sangue com o anticoagulante.
HEMOGRAMA
O hemograma é o exame que avalia o número e a qualidade das células sanguíneas. É utilizado para avaliar o estado geral da ave, a saúde e doença do indivíduo, monitorar a resposta e evolução do paciente em terapia, e o seu prognóstico. No hemograma são avaliados os eritrócitos, os leucócitos e os trombócitos. Compreende o eritrograma, o leucograma e a avaliação dos trombócitos.
O hemograma é utilizado para obter o diagnóstico e monitorar as anemias, como as anemias regenerativas e não regenerativas, anemias hemolíticas e hemorrágicas; diagnóstico dos hemoparasitos; presença de inflamação e doenças mielo e linfoproliferativas (leucemias) e a avaliação do estresse
A amostra para o hemograma é o sangue total, coletado com anticoagulante.
Os parâmetros e as respectivas técnicas estão descritos a seguir.
Processamento da amostra de sangue para hemograma
- Fazer a extensão sanguínea imediatamente após a coleta de sangue
- Manter a amostra de sangue total sob refrigeração até o processamento da amostra
- A extensão da capa leucocitária (camada branca de leucócitos, visível no tubo de microhematócrito após a centrifugação) pode ser feita para observar a morfologia das células (leucócitos), pesquisa de hemoparasitas e bactérias
- Corantes hematológicos para coloração das lâminas: Wright, May-Grünwald Giemsa, corantes seletivos para os leucócitos
HEMOGRAMA
Eritrograma
Hematócrito – 12.000 g (13.700 rpm) por 5 minutos
Hemoglobina – técnica da cianometahemoglobina – leitura em espectrofotômetro
número de eritrócitos
Índices hematimétricos
Volume Globular Médio (VGM)
Fórmula: VGM = Hematócrito x 10 / número de eritrócitos
Concentração de Hemoglobina Globular Média (CHGM)
Fórmula: CHGM = hemoglobina x 100 / hematócrito
LEUCOGRAMA
Número total de leucócitos
Contagem diferencial de leucócitos
LEITURA DA EXTENSÃO SANGUÍNEA:
morfologia, tamanho, coloração, parasitas, bactérias, corpúsculos de inclusão, avaliação dos trombócitos
Estimativa do número de TROMBÓCITOS
tÉCNICAS
- Hematócrito ou Volume globular (VG) – “Packed Cell Volume” (PCV)
- homogeneizar o sangue total
- preencher 2/3 do tubo capilar de microhematócrito
- fechar uma das extremidades do tubo capilar
- centrifugar na centrífuga de microhematócrito (12.000 rpm) por 5 minutos
- fazer a leitura no cartão de microhematócrito (%)
Após a centrifugação, observar a cor e o aspecto do plasma.
Cor: incolor, amarelo-claro, róseo (hemolisado)
Aspecto: límpido, levemente turvo, turvo, lipemico (branco e turvo)
Nas aves saudáveis o plasma é amarelo palha e levemente turvo.
- CONTAGEM de ERITRÓCITOS e LEUCÓCITOS
Método manual – em Câmara de Neubauer
Diluição com o corante supra vital Azul de cresil brilhante
- Preparo da solução de azul de cresil brilhante:
50 mL de soro fisiológico
- µL de azul de cresil brilhante
2.1) Diluição do sangue
- homogeneizar a amostra de sangue
- diluir a amostra em tubo de ensaio (diluição 1:100):
- 1000 µL (1,0 mL) da solução de azul de cresil previamente preparada
- 10 µL de sangue total
- homogeneizar
- aguardar 5 a 10 minutos
- preencher a Câmara de Neubauer (espelhada), aguardar 5 minutos
- fazer a contagem no microscópio ótico (objetiva de 20X), com pouca iluminação
2.2) Contagem na Câmara de Neubauer
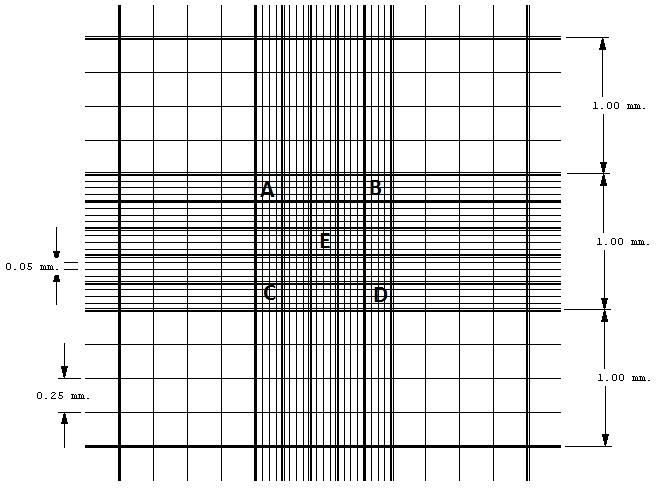
- nas aves a contagem de eritrócitos e de leucócitos é realizada no quadrado grande central da câmara (Figuras 1 e 2)
- contagem de eritrócitos: no quadrado grande central da câmara = contar todos os eritrócitos (Figura 3) nos cinco quadrados pequenos (letras A, B, C, D e E na figura 1), localizados no quadrado grande central. Somar e X 5.000. A leitura pode ser realizada em diagonal, em cinco quadrados pequenos. Resultado: número de eritrócitos /µL
- contagem de leucócitos: os leucócitos coram-se de azul e são esféricos (Figura 3). Contar todos os leucócitos no quadrado grande central, somar e X 1.000. Resultado: número de leucócitos / µL
Figura 1: Retículo da Câmara de Neubauer. O quadrado grande central tem 25 quadrados pequenos. Os eritrócitos de aves são contados em CINCO desses quadrados (letras A, B, C, D e E). Contar todos os leucócitos (aves) presentes no quadrado grande central.
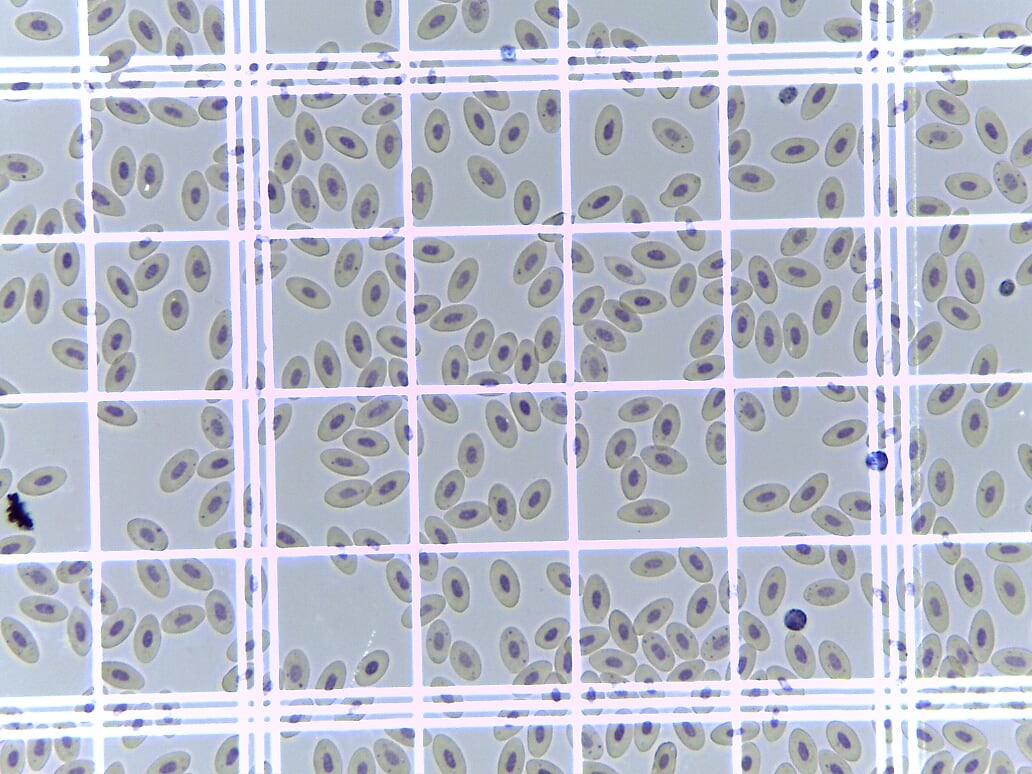
Figura 2: Retículo da câmara de Neubauer, com células sanguíneas de aves. O quadrado grande central tem 25 quadrados pequenos.
Figura 3. Um quadrado pequeno ampliado, do quadrado grande central, delimitado por linhas triplas. Observar os eritrócitos e dois leucócitos esféricos (corados em azul).
- HEMOGLOBINA
Método da cianometahemoglobina
Utilizar kit comercial para determinação da hemoglobina e kit padrão de hemoglobina
Equipamento necessário: espectrofotômetro
Técnica:
- preparar dois tubos, um tubo branco com 2,5 mL de reagente de hemoglobina
- Tubo com amostra
2,5 mL de reagente de hemoglobina (kit comercial)
10 µL de sangue total (amostra previamente homogeneizada)
- Aguardar 5 minutos
- centrifugar o tubo antes da leitura no espectrofotômetro. Centrifugar o tubo a 3000 rpm por 5 minutos. A centrifugação é necessária para que os núcleos dos eritrócitos não interfiram na leitura. Depois da centrifugação fazer a leitura no espectrofotômetro – leitura a 540 nm (520-550).
- LEITURA DA EXTENSÃO SANGUÍNEA CORADA
- na extensão sanguínea corada é realizada a contagem diferencial de leucócitos, a avaliação dos eritrócitos, contagem de trombócitos e a pesquisa de hemoparasitos
- avaliar os eritrócitos: cor, presença de inclusões, eritrócitos imaturos (metarubrócitos, policromatófilos)
- IMPORTANTE: observar o número de policromatófilos por campo. Nas aves anêmicas, o aumento do número de policromatófilos no sangue indica aumento da eritropoese e ocorre nas anemias regenerativas; observar presença de eritrócitos imaturos, como os metarubrócitos)
- leucócitos: tipos, presença de células imaturas, inclusões
- contagem diferencial de leucócitos: contar 100 leucócitos em microscópio óptico e objetiva de imersão (100 X).
- Identificar os leucócitos: heterófilos, eosinófilos, basófilos, monócitos e linfócitos. Contar 100 leucócitos e estabelecer a porcentagem de cada um (contagem relativa, em %)
- observar a presença de heterofilos imaturos (bastonete, metamielócito ou mielócito). O aumento dessas células no sangue é denominado de desvio nuclear dos heterofilos à esquerda e indica inflamação
- observar a morfologia dos heterófilos, presença de heterófilos tóxicos
- avaliar os trombócitos: contar o número de trombócitos por campo, observar a morfologia.
A identificação das células sanguíneas está descrita no tópico “células sanguíneas”, com as fotos.